Сюань Вин Тран, DDS, M.Sc, Ph.D и д-р Лан Тхи Куин Нго, DDS, M.Sc, Ph.D, стоматологический факультет Вьетнамского национального университета медицины и фармацевтики (Хошимин, Вьетнам); проф. Чилало Букпесси, DDS, M.Sc, Ph.D, лаборатория патологии полости рта, визуализации и биотерапии стоматологического факультета Парижского университета (Франция); отделение стоматологии больницы общественной помощи в Париже и больницы Шарля Фуа в Иври-сюр-Сен (Франция).
Для постоянных зубов с обратимым пульпитом в первую очередь показана терапия витальной пульпы, включая прямое покрытие пульпы, а также частичную и полную пульпотомию. При необратимом пульпите часто прибегают к эндодонтическому лечению. В данной статье представлен отчет о двух клинических случаях полной пульпотомии с использованием материала Biodentine™ (Septodont, Сен-Мор-де-Фоссе, Франция) для лечения зрелых постоянных зубов с необратимым пульпитом и острым апикальным периодонтитом. На прицельной рентгенограмме обнаружилось глубокое кариозное поражение с распространением в область пульпы, с рентгенопрозрачным апикальным поражением и увеличением ширины периодонтальной щели. В качестве радикального лечения была выбрана полная пульпотомия с использованием цемента на основе трикальция силиката. После удаления разрушенной ткани с изоляцией коффердамом обнаженная ткань пульпы была ампутирована с использованием нового стерильного бора до уровня отверстия канала зуба. Для закрытия пульпы после достижения гемостаза и для временной реставрации применялся Biodentine™. После лечения клинические симптомы заболевания быстро исчезли. Через один месяц коронковая часть временной реставрации была удалена и поверх защитного покрытия выполнена постоянная композитная реставрация. При наблюдении в течение двух лет симптомы заболевания отсутствовали. На рентгенограммах наблюдалось заживление периапикального поражения и периодонтальной связки. В случаях со зрелыми постоянными зубами с необратимым пульпитом и апикальным периодонтитом полная пульпотомия с применением Biodentine™ может применяться как альтернатива эндодонтическому лечению.
ВВЕДЕНИЕ
Сохранение витальности пульпы зуба является одной из важнейших задач современной стоматологии, которая основывается на концепции минимальной инвазивности. Пульпа зуба обладает способностью к восстановлению в зависимости от интенсивности ее повреждения и степени воспаления. В поддержании жизнеспособности комплекса «дентин-пульпа» участвуют два регенеративных механизма, а именно, третичный реакционный дентиногенез и репаративный дентиногенез. В случае кариозного поражения с относительно медленным прогрессированием, молекулы, которые изначально достигают ткани пульпы, могут вызывать регенерацию дентина.1 Дентин может регенерировать в виде одонтобластов, которые располагаются на периферии зрелой пульпы и отвечают исключительно за синтез дентина. Они могут увеличивать секреторную активность, в результате производя толстый слой реакционного дентина. Этот слой имеет много общего с первичным и вторичным физиологическим дентином и защищает ткань пульпы. Реакционный синтез дентина активируется небольшим количеством провоспалительных цитокинов и (или) биологически активных молекул, ответственных за индукцию эмбриональной дифференциации одонтобластов, таких как TGF или BMP.2 Формирование реакционного дентина подавляется интенсивным воспалением.3 В ответ на тяжелое поражение, такое как быстро прогрессирующий кариес, первичные одонтобласты погибают.4 Предполагается, что это происходит из-за бактериальных токсинов-компонентов, которые высвобождаются из деминерализованного дентина или локальной выработки провоспалительных медиаторов в большом количестве. Однако впоследствии, если условия становятся благоприятными (например, если кариозная инфекция контролируется или устраняется), стволовые клетки / клетки-предшественники в пульпе получают сигнал воздействовать на место поражения и дифференцироваться в одонтобластоподобные клетки. Эти клетки наслаивают матрицу третичного репаративного дентина, по некоторым данным, со скоростью первичного дентиногенеза, что приводит к клиническому результату в виде образования дентинного мостика.5
Терапия витальной пульпы (ТВП), которая включает прямое защитное покрытие пульпы и частичную или полную пульпотомию обнаженной пульпы в кариозных зубах, является общепринятым малоинвазивным методом.6,7 До недавнего времени показанием для проведения ТВП являлся обратимый пульпит несформированных и сформированных зубов при отсутствии патологии в периапикальной области. Постоянные зубы с закрытым апексом и необратимым пульпитом в большинстве случаев требуют проведения нехирургического эндодонтического лечения. Если добавляются признаки и симптомы периапикальной патологии, то нехирургическое эндодонтическое лечение является методом выбора.8,9 В этом случае происходит утрата твердой ткани зуба и препарированный зуб впоследствии ослабляется, что повышает возможность его перелома.10 Кроме того, в некоторых исследованиях отмечается, что фактический уровень неблагоприятных исходов при стандартном лечении корневых каналов в ходе общей практики значительно выше ожидаемого.11–13 Более того, эти методы лечения являются длительным, дорогостоящими и их применение часто приводит к необходимости повторного эндодонтического лечения.14 Поэтому для лечения пульпита можно использовать менее инвазивные альтернативные подходы, даже если пульпит является необратимым.
Результаты многочисленных биологических и клинических исследований показали, что пульпа сформированных зубов, которая обнажается при кариозных поражениях, способна к регенерации, поэтому применение ТВП не следует ограничивать только молочными зубами или зубами без симптоматики. ТВП была предложена как более консервативный подход для лечения зубов с необратимым пульпитом. Благоприятный исход такого лечения зависит от двух факторов: способности оставшейся витальной пульпы к заживлению и биосовместимости агентов, используемых для защитного покрытия пульпы.15–18
Минеральный триоксидный агрегат (МТА) является оптимальным вариантом для выполнения ТВП на зубах с закрытым апексом.19–21 Способность МТА индуцировать репаративный дентиногенез была хорошо продемонстрирована в исследованиях на животных, где при механическом вскрытии пульпы выполнялось прямое защитное покрытие.22,23 По сравнению с гидроксидом кальция МТА индуцирует формирование дентина с большей скоростью и с лучшим качеством структуры.24 Однако было высказано много претензий относительно сложности обработки и смешивания МТА, длительного времени его затвердевания, а также изменения оттенка зубов с течением времени.25 С целью устранения недостатков МТА,28 было разработано несколько новых материалов на основе силиката кальция.26,27
В число этих материалов входит Biodentine™, который, как утверждается, может применяться в качестве материала для замены дентина, в дополнение к эндодонтическим показаниям, аналогичным показаниям для MTA. Biodentine™ не содержит смол и в основном состоит из чистого трикальция силиката, который может затвердевать во влажной среде.29 Было продемонстрировано, что Biodentine™ индуцирует одонтобластическую дифференциацию стволовых клеток пульпы зуба и способствует образованию более однородных и толстых дентинных мостиков с меньшей воспалительной реакцией и меньшим некрозом ткани пульпы по сравнению с гидроксида кальция.23,30 Роль ТВП в лечении заболеваний пародонта постоянных зубов с необратимым пульпитом у взрослых пациентов является неоднозначной. На примере двух клинических случаев, представленных в данной статье, продемонстрированы результаты проведения полной пульпотомии с использованием материала Biodentine™ при лечении постоянных зубов с необратимым пульпитом и периапикальным поражением/увеличением ширины периодонтальной щели.
КЛИНИЧЕСКИЙ СЛУЧАЙ № 1
Пациентка 40 лет обратилась по поводу самопроизвольной продолжительной боли при жевании в зубе 45, возникшей один месяц назад. По результатам клинического обследования в причинном зубе выявлено обширное кариозное поражение, также отмечалась чувствительность к перкуссии. На прицельной рентгенограмме визуализировалось глубокое кариозное поражение, затрагивающее пульпу, а также полупрозрачное апикальное поражение (рис. 1). На основании клинического обследования и рентгенологического исследования был поставлен диагноз «симптоматический необратимый пульпит». Пациентка согласилась на план лечения, включавший полную пульпотомию.
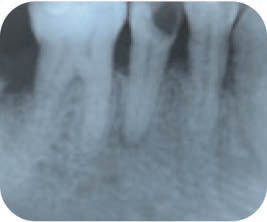
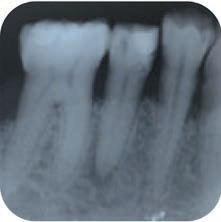
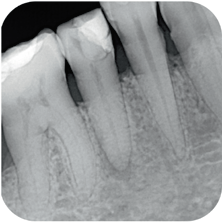
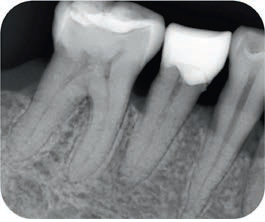
Рис. 1. Прицельные рентгенограммы: a – до вмешательства; b – после лечения; c – через 6 мес после вмешательства; d – через 12 мес после вмешательства
Перед установкой коффердама для изоляции зуба выполнили анестезию (2 % лидокаина гидрохлорид с адреналином 1:100 000, Septodont, Сен-Мор-де-Фоссе, Франция). Операционное поле продезинфицировали марлей, смоченной 5 % раствором гипохлорита натрия (NaOCl). Пораженную ткань удалили с помощью стерилизованного круглого высокоскоростного бора с водяным охлаждением. Затем провели ампутацию обнаженной ткани пульпы стерилизованным круглым высокоскоростным бором до уровня отверстия канала. Кровотечение было остановлено примерно через две минуты с помощью стерильного ватного тампона, смоченного 2,5 % раствором гипохлорита натрия.
Затем полость заполнили материалом Biodentine™ (Septodont, Сен-Мор-де-Фоссе, Франция) приготовленного с помощью амальгамтрегера и плаггера (рис. 2). Пациентке было рекомендовано прийти через один месяц при условии отсутствия прогрессирующей боли.
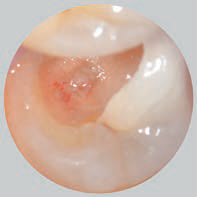
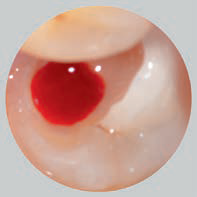
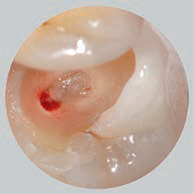
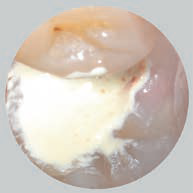
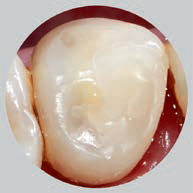
Рис. 2. Фотографии полости рта: a–c – доступ для проведения пульпотомии; d – внесение метериала Biodentine™; e – композитная реставрация
На следующем приеме пациентка сообщила, что в первый день после лечения отмечалась легкая боль, которая вскоре прошла. Кроме того, при вертикальной перкуссии болевых ощущений не было. Поверхностный слой Biodentine™ удалили, оставив примерно 3 мм материала. Окончательная реставрация зуба была выполнена композитом (3M ESPE, Сент-Пол, Миннесота, США). Клиническое обследование и рентгенологическое исследование провели через 6 мес и 1 год после операции (см. рис. 1). Пациентка не предъявляла жалоб на данный зуб, реакция на холодовой тест и электростимуляцию пульпы была отрицательной, на прицельных рентгенограммах периапикального поражения не отмечалось. В ходе контрольного рентгенологического исследования через 6 мес выявили нарушение краевого прилегания, поэтому приняли решение заменить реставрацию на композитную накладку.
КЛИНИЧЕСКИЙ СЛУЧАЙ № 2
Пациентка 25 лет обратилась по поводу сильной самопроизвольной и продолжительной боли в области зуба 36, которая возникала при жевании и употреблении холодных напитков несколько раз в течение двух предшествующих недель. В ходе клинического обследования был обнаружен кариес, распространяющийся на ткань пульпы, зуб также был чувствителен к вертикальной и горизонтальной перкуссии. На прицельной рентгенограмме наблюдалось увеличение ширины периодонтальной щели у мезиального корня зуба (рис. 3). Был диагностирован «необратимый пульпит».
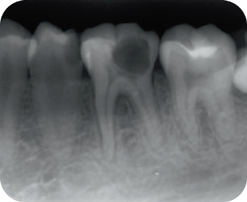
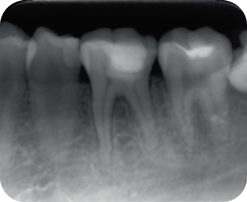
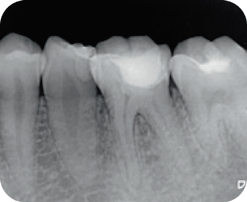
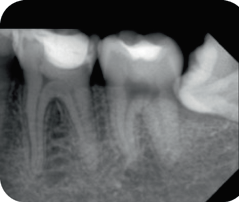
Рис. 3. Прицельные рентгенограммы: a – до вмешательства; b – после лечения; c – через 6 мес после вмешательства; d – через 24 мес после вмешательства
После получения информированного согласия от пациентки была проведена та же процедура, что описана в клиническом случае № 1. Коронковая пульпа была удалена до уровня отверстий каналов. Подтверждено кровотечение из всех отверстий каналов корней зуба. После достижения гемостаза полость зуба была заполнена материалом Biodentine™ в качестве защитного покрытия и временной реставрации.
Пациентка сообщила о слабой боли в день вмешательства, которая уменьшилась на следующий день. Спустя один месяц у пациентки отсутствовал дискомфорт при жевании, хотя при вертикальной перкуссии отмечались незначительные болевые ощущения. Поверхностный слой Biodentine ™ был удален, затем выполнена постоянная композитная реставрация зуба. Через 6 мес чувствительность к перкуссии отсутствовала, а состояние пространства периодонтальной связки улучшилось. Результаты обследования, выполненного через 24 мес, показали, что пространство периодонтальной связки вернулось к нормальному состоянию, симптомы поражения зуба отсутствовали, наблюдались отрицательные реакции на холодовую пробу и электростимуляцию пульпы.
ОБСУЖДЕНИЕ
До недавнего времени в случаях с необратимым пульпитом применялось эндодонтическое лечение. Нехирургическое эндодонтическое лечение считается инвазивным и небиологическим методом, так как при этом удаляется вся воспаленная, инфицированная и здоровая пульпа, что ведет к потере ее репаративного/регенеративного потенциала, ее собственных свойств и иннервации.31 Поэтому для лечения зубов с необратимым пульпитом был предложен более консервативный подход с использованием ТВП.15–18
Успешный исход в обоих представленных клинических случаях дает дополнительные клинические доказательства эффективности полной пульпотомии при лечении зубов с клиническими признаками и симптомами необратимого пульпита и апикальным периодонтитом. Taha и соавт. (2017) указывают, что показатель успешного исхода при пульпотомии с применением MTA для зрелых постоянных зубов с кариозным обнажением пульпы составил 100 % при наблюдении в течение одного года и 92,7 % через три года.20 В другом проспективном исследовании материала Biodentine™ с выполнением полной пульпотомии для зрелых постоянных зубов с необратимым пульпитом авторы обнаружили высокий клинический показатель успешного исхода через один год, близкий к 100 %, а также показатель успешного исхода на основании рентгенографического исследования до 93,8 %.32 Cushley и соавт. (2019) в систематическом обзоре оценивали клинический показатель успешного исхода полной пульпотомии при лечении постоянных зубов с признаками и симптомами необратимого пульпита. Они обнаружили, что показатель успешного исхода при полной пульпотомии при наблюдении в течение 12 мес составил 97,4 % по клиническим результатам и 95,4 % по рентгенологическим данным.33 Однако целесообразность ТВП для лечения зрелых постоянных зубов с необратимым пульпитом и периапикальным поражением остается неоднозначной.
В представленных в данной статье отчетах о клинических случаях у взрослых пациентов наблюдалась самопроизвольная длительная боль и чувствительность к перкуссии, которые давно считаются клиническими предикторами стадии необратимого поражения пульпы.34 Кроме того, на рентгенограммах этих зубов отмечалось обширное кариозное поражение, а также апикальное поражение или расширение пространства периодонтальной связки. В обоих случаях через один месяц после полной пульпотомии с применением Biodentine™ произошло клиническое улучшение. Также положительный результат зафиксирован на рентгенограммах. В первом случае апикальное рентгенопрозрачное поражение улучшилось через 6 мес и полностью пришло в норму через 12 мес. Ширина периодонтальной щели во втором случае пришло в нормальное состояние через 6 мес.
Ткань пульпы может сохранять витальность даже в зубах с диагностированным на рентгенограмме поражением в периапикальной области; у витальной пульпы есть потенциал для восстановления в присутствии подходящего материала.35 Периапикальные воспалительные реакции связаны с диффузией бактериальных продуктов в периапикальную ткань, что ведет к сложному взаимодействию воспалительных медиаторов, цитокинов и нейропептидов.35 Результаты исследований продемонстрировали, что апикальный периодонтит может ассоциироваться с необратимым пульпитом. Апикальный периодонтит на рентгенограммах необязательно означает некротизацию пульпы. Воспаленная витальная пульпа зуба вызывает иммунологическую реакцию, которая может стать причиной локальных изменений в периапикальной соединительной ткани.17,36,37 Таким образом, клинические признаки и симптомы, имеющиеся у пациента, не отражают фактическую степень воспаления в ткани пульпы. Помимо этого в нескольких исследованиях было продемонстрировано излечение зубов с необратимым пульпитом и периапикальным поражением после терапии витальной пульпы.11,18,32 Расширение периодонтальной связки на фоне инфекции было зарегистрировано в зубах с пульпитом, поражениями пульпы и периапикальной области или даже при витальной пульпе с минимальной гиперемией.38,39 Однако лечение расширения периодонтальной связки в зубах с необратимым пульпитом в более ранних исследованиях упоминалось редко.
Точная клиническая диагностика имеет важное значение для назначения ТВП, однако было показано, что при клиническом обследовании ставится только временный диагноз, который может быть неверным.40,41 В качестве дополнительного диагностического показателя для оценки степени воспаления и потенциала заживления оставшейся ткани пульпы был предложен контроль кровотечения после удаления инфицированной ткани пульпы.15,42 Возможность контроля кровотечения в течение 5–10 мин указывает на наличие воспаления пульпы легкой или средней степени тяжести и возможность ее заживления в благоприятных условиях.18 В обоих случаях кровотечение возникло в течение 2 мин, что может быть показанием к проведению ТВП.
В представленных в данной статье клинических случаях материал Biodentine™ использовался в качестве защитного покрытия пульпы. В проведенных авторами более ранних исследованиях in vivo было продемонстрировано, что Biodentine™ обеспечивает оптимальную среду для заживления пульпы, индуцируя образование однородного дентинного мостика в месте повреждения при прямом нанесении на механически вскрытую пульпу у крыс. Известно, что факторы роста, ассоциированные с матрицей дентина, могут посылать мезенхимальным стволовым клеткам в пульпе сигнал о необходимости дифференцироваться в одонтобластоподобные клетки и создавать непрерывный по отношению к первичному дентину минерализованный барьер, который защищает расположенную ниже витальную ткань пульпы.23,43
Результаты гистологического исследования показали, что в ткани пульпы, находящейся в нескольких миллиметрах от некротизированной пульпы с бактериальной колонизацией, обычно отсутствует воспалительный процесс и бактерии.41 Корневая пульпа воспаляется редко. Поэтому сразу после удаления инфицированной и воспаленной ткани и нанесения подходящего защитного покрытия создается благоприятная среда для заживления раны пульпы. В дополнение к хорошим герметизирующим свойствам Biodentine™, как и другие цементы с трикальций силикатом в составе, может контролировать выработку провоспалительного фактора и снижать рекрутинг воспалительных клеток.44
Длительный неблагоприятный исход после терапии витальной пульпы и эндодонтического лечения объясняется в основном микроутечками на границе коронковой части зуба и реставрации. Massler и соавт. (1978) продемонстрировали, что наиболее важной причиной длительного неблагоприятного исхода ТВП является наличие утечки в ходе процесса заживления.45 Biodentine™ продемонстрировал хорошую герметизирующую способность, устойчивость к микроутечкам,46 а прочность его сцепления с композитным материалом увеличилась в течение двухнедельного периода заживления.47 Было показано, что Biodentine™ обеспечивает лучшее время отверждения, обработку и механические свойства по сравнению с MTA.48 Этот цемент можно успешно применять в стоматологии в качестве реставрационного материала на период до 6 мес и в качестве заменителя дентина под композитный материал при реставрации жевательных зубов.49
Оценка успешного исхода при проведении ТВП основана на клиническом и рентгенологическом наблюдении. Симптомы поражения зуба должны отсутствовать. Ожидается, что зуб с полной пульпотомией не будет реагировать при пробах на чувствительность. Однако реакция должна быть положительной в случае защитного покрытия пульпы или частичной пульпотомии. Отрицательная реакция не указывает на некроз пульпы. Успешность исхода лечения определяется как отсутствие симптомов и сохранение витальности пульпы в течение минимум одного года.50
ВЫВОДЫ
На основании перспектив применения биоактивного материала и изучения биологии пульпы, полная пульпотомия при лечении постоянных зубов взрослых пациентов с необратимым пульпитом и апикальным периодонтитом или увеличение ширины периодонтальной щели может рассматриваться как альтернатива эндодонтическому лечению. Для подтверждения преимуществ этого варианта лечения требуются долгосрочные исследования.
ЛИТЕРАТУРА:
- Smith, A.J.; Cassidy, N.; Perry, H.; BegueKirn, C.; Ruch, J.-V.; Lesot, H. Reactionary dentinogenesis. Int. J. Dev. Biol. 2003, 39, 273–280.
- Bleicher, F. Odontoblast physiology. Exp. Cell Res. 2014, 325, 65–71. .
- Cooper, P.R.; Takahashi, Y.; Graham, L.W.; Simon, S.; Imazato, S.; Smith, A.J. Inflammation–regeneration interplay in the dentine–pulp complex. J. Dent. 2010, 38, 687–697.
- Bjørndal, L. Indirect pulp therapy and stepwise excavation. Pediatric Dent. 2008, 30, 225–229.
- Farges, J.-C.; Alliot-Licht, B.; Renard, E.; Ducret, M.; Gaudin, A.; Smith, A.J.; Cooper, P.R. Dental pulp defence and repair mechanisms in dental caries. Mediat. Inflamm. 32015, 2015, 230251.
- Chin, J.; Thomas, M.; Locke, M.; Dummer, P. A survey of dental practitioners in Wales to evaluate the management of deep carious lesions with vital pulp therapy in permanent teeth. Br. Dent. J. 2016, 221, 331–338.
- Schwendicke, F.; Stolpe, M. Direct pulp capping after a carious exposure versus root canal treatment: A cost-effectiveness analysis. J. Endod. 2014, 40, 1764–1770.
- American Academy of Pediatric Dentistry. Guideline on pulp therapy for primary and immature permanent teeth. Pediatr. Dent. 2009, 31, 179–186.
- American Association of Endodontists. Endodontic Diagnosis. Endodontics: Colleagues for Excellence; MediVisuals, Inc.: Richmond, VA, USA, 2013.
- Al-Omiri, M.K.; Mahmoud, A.A.; Rayyan, M.R.; Abu-Hammad, O. Fracture resistance of teeth restored with post-retained restorations: An overview. J. Endod. 2010, 36, 1439–1449.
- Bjørndal, L.; Reit, C. Endodontic malpractice claims in Denmark 1995–2004. Int. Endod. J. 2008, 41, 1059–1065.
- Tavares, P.B.; Bonte, E.; Boukpessi, T.; Siqueira, J.F., Jr.; Lasfargues, J.-J. Prevalence of apical periodontitis in root canal–treated teeth from an urban French population: Influence of the quality of root canal fillings and coronal restorations. J. Endod. 2009, 35, 810–813.
- Boucher, Y.; Matossian, L.; Rilliard, F.; Machtou, P. Radiographic evaluation of the prevalence and technical quality of root canal treatment in a French subpopulation. Int. Endod. J. 2002, 35, 229–238.
- Figdor, D. Apical periodontitis: A very prevalent problem. Oral Surg. Oral Med. Oral Pathol. Oral Radiol. Endod. 2002, 94, 651–652.
- Matsuo, T.; Nakanishi, T.; Shimizu, H.; Ebisu, S. A clinical study of direct pulp capping applied to cariousexposed pulps. J. Endod. 1996, 22, 551–556.
- Aguilar, P.; Linsuwanont, P. Vital pulp therapy in vital permanent teeth with cariously exposed pulp: A systematic review. J. Endod.2011, 37, 581–587.
- Asgary, S.; Eghbal, M.J.; Fazlyab, M.; Baghban, A.A.; Ghoddusi, J. Five-year results of vital pulp therapy in permanent molars with irreversible pulpitis: A non-inferiority multicenter randomized clinical trial. Clin. Oral Investig. 2015, 19, 335–341.
- Taha, N.A.; Ahmad, M.B.; Ghanim, A. Assessment of mineral trioxide aggregate pulpotomy in mature permanent teeth with carious exposures. Int. Endod. J. 2017, 50, 117–125. [CrossRef].
- Witherspoon, D.E. Vital pulp therapy with new materials: New directions and treatment perspectives-Permanent teeth. Pediatric Dent. 2008, 30, 220–224.
- Taha, N.A.; Khazali, M.A. Partial pulpotomy in mature permanent teeth with clinical signs indicative of irreversible pulpitis: A randomized clinical trial. J. Endod. 2017, 43, 1417-1421.
- Kundzina, R.; Stangvaltaite, L.; Eriksen, H.; Kerosuo, E. Capping carious exposures in adults: A randomized controlled trial investigating mineral trioxide aggregate versus calcium hydroxide. Int. Endod. J. 2017, 50, 924–932.
- Schmitt, D.; Lee, J.; Bogen, G. Multifaceted use of ProRootTM MTA root canal repair material. Pediatr. Dent. 2001, 23, 326–330.
- Tran, X.V.; Gorin, C.; Willig, C.; Baroukh, B.; Pellat, B.; Decup, F.; Opsahl Vital, S.; Chaussain, C.; Boukpessi, T. Effect of a calcium-silicate-based restorative cement on pulp repair. J. Dent. Res. 2012, 91, 1166–1171.
- Simon, S.R.J.; Berdal, A.; Cooper, P.R.; Lumley, P.J.; Tomson, P.L.; Smith, A.J. Dentin-pulp complex regeneration: From lab to clinic. Adv. Dent. Res. 2011, 23, 340–345.
- Camilleri, J. Staining potential of Neo MTA Plus, MTA Plus, and Biodentine™ used for pulpotomy procedures. J. Endod. 2015, 41, 1139–1145.
- Dawood, A.E.; Parashos, P.; Wong, R.H.; Reynolds, E.C.; Manton, D.J. Calcium silicate-based cements: Composition, properties, and clinical applications. J. Investig. Clin. Dent. 2017, 8, e12195.
- Quintana, R.M.; Jardine, A.P.; Grechi, T.R.; Grazziotin-Soares, R.; Ardenghi, D.M.; Scarparo, R.K.; Grecca, F.S.; Kopper, P.M.P. Bone tissue reaction, setting time, solubility, and pH of root repair materials. Clin. Oral Investig. 2019, 23, 1359–1366.
- Vallés, M.; Roig, M.; Duran-Sindreu, F.; Martínez, S.; Mercadé, M. Color stability of teeth restored with Biodentine™: A 6-month in vitro study. J. Endod. 2015, 41, 1157–1160.
- Donfrancesco, O.; Del Giudice, A.; Zanza, A.; Relucenti, M.; Petracchiola, S.; Gambarini, G.; Testarelli, L.; Seracchiani, M. SEM Evaluation of Endosequence BC Sealer Hiflow in Different Environmental Conditions. J. Compos. Sci. 2021, 5, 99.
- Marconyak Jr, L.J.; Kirkpatrick, T.C.; Roberts, H.W.; Roberts, M.D.; Aparicio, A.; Himel, V.T.; Sabey, K.A. A comparison of coronal tooth discoloration elicited by various endodontic reparative materials. J. Endod. 2016, 42, 470–473.
- Wolters,W.; Duncan, H.; Tomson, P.; Karim, I.; McKenna, G.; Dorri, M.; Stangvaltaite, L.; Van Der Sluis, L. Minimally invasive endodontics: A new diagnostic system for assessing pulpitis and subsequent treatment needs. Int. Endod. J. 2017, 50, 825–829.
- Taha, N.A.; Abdelkhader, S.Z. Outcome of full pulpotomy using Biodentine™ in adult patients with symptoms indicative of irreversible pulpitis. Int. Endod. J. 2018, 51, 819–828.
- Cushley, S.; Duncan, H.F.; Lappin, M.J.; Tomson, P.L.; Lundy, F.T.; Cooper, P.; Clarke, M.; El Karim, I.A. Pulpotomy for mature carious teeth with symptoms of irreversible pulpitis: A systematic review. J. Dent. 2019, 88, 103158.
- Bergenholtz, G.; Spångberg, L. Controversies in endodontics. Crit. Rev. Oral Biol. Med. 2004, 15, 99–114.
- Stashenko, P.; Teles, R.; d’Souza, R. Periapical inflammatory responses and their modulation. Crit. Rev. Oral Biol. Med. 1998, 9, 498–521.
- Asgary, S.; Parhizkar, A. The Role of Vital Pulp Therapy in the Management of Periapical Lesions. Eur. Endod. J. 2021, 6, 130.
- Bowles, W.R.; Withrow, J.C.; Lepinski, A.M.; Hargreaves, K.M. Tissue levels of immunoreactive substance P are increased in patients with irreversible pulpitis. J. Endod. 2003, 29, 265–267.
- Chapman, M.N.; Nadgir, R.N.; Akman, A.S.; Saito, N.; Sekiya, K.; Kaneda, T.; Sakai, O. Periapical lucency around the tooth: Radiologic evaluation and differential diagnosis. Radiographics 2013, 33, E15–E32.
- Dayal, P.; Subhash, M.; Bhat, A. Pulpo-periapical periodontitis: A radiographic study. Endodontology 1999, 11, 60–64.
- Lin, L.M.; Ricucci, D.; Saoud, T.M.; Sigurdsson, A.; Kahler, B. Vital pulp therapy of mature permanent teeth with irreversiblenpulpitis from the perspective of pulp biology. Aust. Endod. J. 2020, 46, 154–166.
- Ricucci, D.; Loghin, S.; Siqueira Jr, J.F. Correlation between clinical and histologic pulp diagnoses. J. Endod. 2014, 40, 1932–1939.
- Stanley, H.R. Pulp capping: Conserving the dental pulp—Can it be done? Is it worth it? Oral Surg. Oral Med. Oral Pathol. 1989, 68, 628–639.
- Tran, X.V.; Salehi, H.; Truong, M.T.; Sandra, M.; Sadoine, J.; Jacquot, B.; Cuisinier, F.; Chaussain, C.; Boukpessi, T. Reparative mineralized tissue characterization after direct pulp capping with calcium-silicatebased cements. Materials 2019, 12, 2102.
- Giraud, T.; Jeanneau, C.; Bergmann, M.; Laurent, P.; About, I. Tricalcium silicate capping materials modulate pulp healing and inflammatory activity in vitro. J. Endod. 2018, 44, 1686–1691.
- Massler, M. Preserving the exposed pulp: A review. J. Pedod. 1978, 2, 217–227.
- Atmeh, A.; Chong, E.; Richard, G.; Festy, F.;Watson, T. Dentin-cement interfacial interaction: Calcium silicates and polyalkenoates. J. Dent. Res. 2012, 91, 454–459.
- Ha, H.-T. The effect of the maturation time of calcium silicate-based cement (Biodentine ™) on resin bonding: An in vitro study. Appl. Adhes. Sci. 2019, 7, 1–13.
- Pradelle-Plasse, N.; Tran, X.V.; Colon, P.; Laurent, P.; Aubut, V.; About, I.; Goldberg, M. Emerging trends in (bio) material research. In Biocompatibility or Cytotoxic Effects of Dental Composites, 1st ed.; Coxmoor Publishing Company: Oxford, UK, 2009; pp. 181–203.
- Koubi, G.; Colon, P.; Franquin, J.-C.; Hartmann, A.; Richard, G.; Faure, M.-O.; Lambert, G. Clinical evaluation of the performance and safety of a new dentine substitute, Biodentine™, in the restoration of posterior teeth—A prospective study. Clin. Oral Investig. 2012, 17, 243–249.
- El-Karim, I.; Kundzina, R.; Krastl, G.; Dammaschke, T.; Fransson, H. European Society of Endodontology position statement: Management of deep caries and the exposed pulp. Int. Endod. J. 2019, 52, 923–934.
Biodentine™
Biodentine можно использовать в любых клинических ситуациях, когда поврежден дентин, как в области коронки зуба, так и в области корня:
- в области коронки: временное восстановление эмали, постоянное восстановление дентина, глубокие или крупные кариозные полости, глубокие пришеечные или радикулярные поражения, покрытие пульпы, пульпотомия (обратимый и необратимый пульпит).
- в области корня: перфорации корня и бифуркации, внутренняя/внешняя резорбция, апексификация, ретроградное хирургическое пломбирование.
Biodentine в Россию эксклюзивно поставляет компания STI DENT ►
► 53